發布時間:2016-03-18 文章來源:識林-柯 識林
2016年3月9-10日,北京大學連續制造研討會在北京大學舉行。本次研討會系統性介紹討論了連續制造的最新發展和實踐案例,20位報告人來自連續制造領域全球領先的制藥企業和設備生產企業的實際負責人,以及美國、歐盟和我國藥監機構的代表。包括原料藥連續制造領先企業GSK先進制造負責人、End-to-End技術首創者瑞士Novartis連續制造團隊負責人,首個使用連續制造技術在FDA獲批產品的Vertex連續制造負責人,以及來及Pfizer, Merck, Lilly, BMS的連續制造團隊負責人和設備支持商GEA,同時還有來自國內的生物制品連續灌流技術企業廣州銘康和連續噴霧凍干設備制造商東富龍的團隊負責人。會議內容體現了目前國際藥品連續制造領域的最高水準,共有160余位來自國內外制藥業界、學界和監管機構的同行參會。

連續制造勢在必行
對比其他行業的生產效率,制藥業顯然已經落后于其他行業 1 。
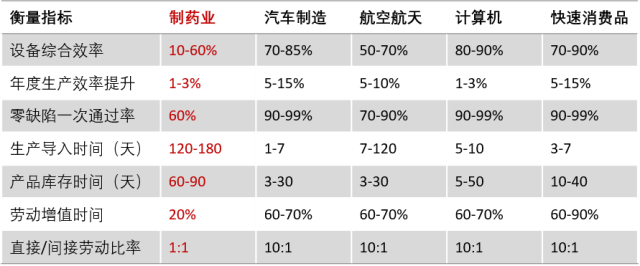
隨著競爭的白熱化和資本市場的沖擊融合,品牌藥企業也不得不開始關注如何通過提高生產技術水平來提高效率和質量。連續制造可能帶來的優勢,如生產迅捷、設計靈活、無需放大、數據有效、質量穩定、以及縮短供應鏈等 ,使得先進制藥技術越來越有吸引力。研討會的報告人來自10家連續制造頂尖企業,分別在原料藥連續制造、供臨床制劑的連續制造、端到端(End-to-End)制劑連續制造、固體口服制劑和生物制品的連續制造上分享最新進展,9個實踐案例分析分別從基建工程、模塊化設計、控制策略、工藝開發、產品組合設計和設備支持等方面詳細闡述了連續制造在應用層面的問題。
Vertex的制劑與工藝副總裁、連續制造團隊負責人Thomas Hayden博士就在報告中提到,目前已獲批產品的工藝能力能達到9-10個sigma,Cpk能達到11。Novartis的連續制造負責人Markus Krumme博士也表示,Novartis目標是未來至少50%的化學合成通過連續制造工藝完成,至少90%的口服固體制劑通過連續制造工藝生產。“盡管總是有例外,總是有不適用連續制造工藝的產品,但我們會將連續制造的科技應用在盡可能多的產品上,因為基于企業的評估,這確實能帶來長期成本的降低和效率的提高”
監管機構擁抱藥品制造新科技
研討會期間,來自美國、歐盟的監管機構代表表示,現有的法律法規框架支持連續制造工藝,FDA的Larry Lee博士介紹,目前在FDA有專門新興技術團隊(ETT),負責研究及與企業探討新興技術的應用和監管對接。討論中業界的代表也表示,企業歡迎FDA現場考察。2015年7月,FDA已經批準了第一個使用連續制造技術生產的藥品ORKAMBITM 。來自歐盟監管機構的代表Leticia Peyrat博士在報告中也介紹,雖然EMA目前沒有只針對連續制造的指南,但ICH Q8-Q11,工藝驗證、實時放行等指南,以及歐洲藥典中論述化學計量學內容的章節,都是企業參考的材料,EMA對于先進技術持開放態度,同時也在企業遞交的申請與反饋中總結了有關取樣、設備、維護、IPC等問題。
我國食品藥品監督管理總局藥品審評中心許嘉齊主任到會,做題為《醫藥發展與先進技術》的主題演講,他提到:“不謀萬世者,不足謀一時;不謀全局者,不足謀一域”,不論產業發展還是監管走向,都應該著眼長遠和全局,積極適應新技術和新變化,但同時也要從產品特性的角度出發,不做為了“連續”而“連續“的創新。

研討會的聯席組長,曾在FDA工作過22年的Moheb Nasr博士在報告中說,不論是對于業界還是監管機構,拒絕都不是應夠的態度,探究新的科技本就是我們這個知識密集型行業中科學家們應該做的事情。目前的過渡階段,連續制造和批次生產沒有那么不同。首先,很多公司是連續制造工藝與批次生產工藝糅合(hybrid)的。其次,批次生產中也運用連續制造工藝,比如連續壓片工藝。第三,質控方面考慮都是相同的,對于產品本身的考量,不因工藝的改變而有所改變。“連續制造”中運用很多“先進制藥科技”,而先進制藥科技不只有連續制造。也正如FDA的ETT不僅支持連續制造,而是一切藥品制造有關的科學和技術。

歐美國家的學術和產業研究已有將近十年時間,研討會上我國藥機設備廠東富龍的張海斌總經理也介紹了國內在噴霧凍干設備制造和模塊化生產的進展,廣州銘康的楊琴總經理也分享了在生物制品連續灌流技術探索和實施上的經驗。
與此同時,在研討會上還提出了諸多問題有關技術和監管對接的問題:
-
對于“批”(Lot/Batch)的定義
-
對于“Flow Processing”中最重要的參數之一流速(Flow Rate)的控制
-
對于駐留時間分布(Residence Time Distribution)的判斷
-
實施放行檢驗(Real Time Releas Test)的方法和考量
-
控制策略
-
物料追溯系統的完善程度
-
對貨架期的定義
-
對于中斷/故障發生后選擇性棄置產品量的選擇
-
監管控制策略Vs.技術控制策略
-
….
挑戰和機遇
對于現有批制造的企業,目前仍然存在已有設備利用、集成人員缺口以及前期投資巨大等挑戰。未來制造現場所需人員將大幅減少,但對操作人員要求更高,可能產生新的職業。裝備不能解決所有問題,操作人員需要在項目前期跟進,理解工藝和產品設計,以便靈活應對生產中可能的出現的狀況。無論是企業還是監管機構,在這一新技術的實踐上,都需要化學工程、處方開發、建模仿真、流程控制、以及傳統藥學的多面復合型人才。
目前我國在先進制藥技術領域起步尚晚,仍待了解學習。推動制藥行業技術發展和革新,需要產業界、學界和監管機構的不斷研究和探索。
來源:GSK先進制造技術部門負責人Mark Buswell博士在PKU CMS的報告
作者:識林-柯

